国内医药外包服务主要相关法律法规
相关报告
- 数据更新中...
(1)国内主要相关法律法规
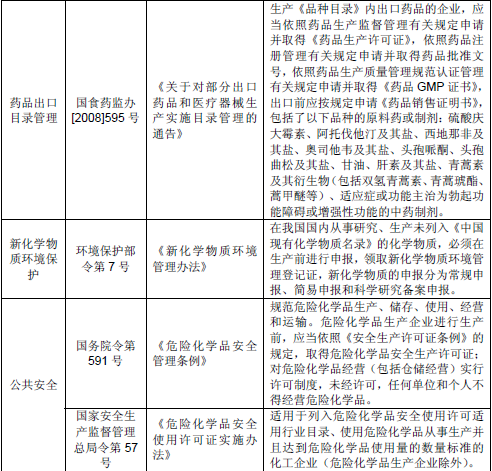
②ICH国际协调会议要求

(2)出口地主要法律法规
①药品法典要求
包括了CFR(CodeofFederalRegulations)美国《联邦规章典籍》第21章“食品与药品”的相关规定以及《欧洲药典》第七版。此外,欧洲议会和欧盟理事会要求从2013年7月开始,所有出口到欧盟的原料药均需出具出口国监管部门的书面声明,以符合欧盟监管要求。
②ICH国际协调会议要求
为了严格管理药品质量,必须对药品的研制、开发、生产、销售等进行控制和审批,从而形成了药品注册制度。但是由于不同国家对药品注册的要求各不相同,这不利于病人在药品安全性、有效性和质量方面得到科学的保证,同时也阻碍了医药事业的发展。1990年由美国、日本和欧盟三方的政府药品注册部门和制药行业共同发起了ICH即人用药物注册技术要求国际协调会议。其推出的ICHQ7已经成为全球原料药生产的共同指南。
本文地址:http://www.zwzyzx.com/show-262-124565-1.html
下一篇:国家医药外包服务主要产业政策
相关资讯
- 全球特色原料药主要产品进口国的竞争情况(2015-05-27)
- 美国医疗资源是医美发展的良好根基(2016-05-04)
- 国内医用敷料行业现状(2015-12-29)
- 发改委:推进医疗服务价格改革(2016-12-06)
- 女性人口基数提升及经济地位的独立成为支撑医美市场高需求的源动力(2016-09-09)
- 国内兽药行业技术状况及经营模式(2015-06-21)
- 我国体外诊断行业主要细分产品的市场占有率(2015-05-23)
- 未来对比剂市场的增长驱动因素(2015-08-25)
合作媒体
最新报告
定制出版
热门报告
免责声明
中为咨询所引述的资料是用于行业市场研究以及讨论和交流,并注明出处,部分内容是由相关机构提供。若有异议请及时联系本公司,我们将立即依据相关法律对文章进行删除或作相应处理。查看详细》》



