国内肿瘤测序第三方检测与医院投放并行
相关报告
- 数据更新中...
国内肿瘤测序行业监管政策与美国的CLIA认证不同,所有的临床应用都要接受卫计委和CFDA的监管。从CFDA和卫计委公布的肿瘤检测临床应用试点单位类型可以大体分为第三方检测机构(独立的医学检验所)和医疗机构两种类型。从商业模式上看,大致可以分为医学检验所(第三方检测)和医院投放两种模式。医院投放模式资产较轻,主要面向的市场是那些有资质和实力自己做肿瘤测序、尤其是有科研需求的医疗机构,采用销售耗材的商业模式。
第三方检测与医院投放对比
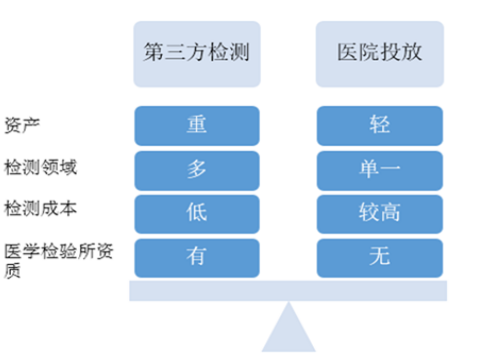
医学检验所是重资产的模式,行业准入门槛很高,虽然它们也申请到了临床应用试点,但是依然还是需要从医院寻找终端需求。目前政策下,医院是肿瘤测序市场的唯一合法入口,但并不排除未来政策环境可以允许医学检验所本身具有采集血样的资质。如果存在这种情况,那么医学检验所就有了直营的商业模式,对于第三方检验来说则会有更好的市场。
本文地址:http://www.zwzyzx.com/show-329-200990-1.html
上一篇:国内肿瘤测序服务商业模式多元
下一篇:肿瘤测序仪决定测序质量
相关资讯
- 国内一次性医疗器械行业技术水平及技术特点(2015-04-27)
- 全球医药行业发展情况(2015-08-25)
- 2015年全球微创手术器械销售额可望达到260 亿~290亿美元的规模(2015-01-09)
- 2013年度天津地区各类医疗卫生机构床位数分析(2014-04-01)
- 医院洁净手术部及其发展趋势(2015-07-17)
- 体外诊断行业竞争情况(2015-12-29)
- 医药研发服务外包的理念日益得到认可(2015-04-21)
- 医疗器械行业全球竞争格局及市场化程度(2016-01-08)
合作媒体
最新报告
定制出版
热门报告
免责声明
中为咨询所引述的资料是用于行业市场研究以及讨论和交流,并注明出处,部分内容是由相关机构提供。若有异议请及时联系本公司,我们将立即依据相关法律对文章进行删除或作相应处理。查看详细》》



