CAR-T:接过癌症免疫治疗大旗
相关报告
- 数据更新中...
T淋巴细胞是肿瘤细胞的天敌,在肿瘤免疫应答中起主要作用,对肿瘤细胞有极强的杀伤作用。但是,使用内源性T细胞进行肿瘤免疫治疗时,靶抗原需经过加工处理后才能和靶细胞表面的主要组织相容性复合物(mainhistocompatibilitycomplex,MHC)作用,也即“MHC限制性”。然而,肿瘤免疫编辑的过程会使MHC在肿瘤细胞表面表达下降,破坏抗原加工过程,降低肽段免疫原性。这样长期形成的免疫逃逸机制,能使肿瘤细胞成功躲避T细胞攻击,肿瘤快速增殖。此外,人体内肿瘤特异性的T细胞数量较少,并且由于大多数肿瘤细胞不断表达自体抗原,使得靶向这些抗原的T细胞通过免疫耐受机制被中和或移除,数量进一步减少。因此,包括细胞因子诱导的杀伤细胞在内的T细胞过继性免疫治疗虽然在部分肿瘤的治疗中取得了一定的效果,但在大多数肿瘤中疗效尚不能令人满意。
CAR-T,全称ChimericAntigenReceptorT-CellImmunotherapy,即嵌合抗原受体T细胞免疫疗法。通过将识别肿瘤相关抗原(tumorassociatedantigen,TAA,是指一些肿瘤细胞表面糖蛋白或糖脂成分,它们在正常细胞上有微量表达,但在肿瘤细胞表达明显增高。)的scFv和胞内信号域“免疫受体酪氨酸活化基序(immunoreceptortyrosinebasedactivationmotifs,ITAM,通常为CD3ζ或FcεRIγ)”在体外进行基因重组,生成重组质粒,再在体外通过转染技术转染到患者的T细胞,使患者T细胞表达肿瘤抗原受体。转染后经过纯化和大规模扩增后的T细胞,也即CAR-T细胞,可以特异性地识别肿瘤相关抗原,使效应T细胞的靶向性、杀伤活性和持久性较常规应用的免疫细胞大幅提高,并可克服肿瘤局部免疫抑制微环境,从而打破宿主免疫耐受状态,杀灭肿瘤细胞。
完整的CAR-T结构包括抗原结合区、跨膜链接区和胞内信号区三个部分。
CAR-T,全称ChimericAntigenReceptorT-CellImmunotherapy,即嵌合抗原受体T细胞免疫疗法。通过将识别肿瘤相关抗原(tumorassociatedantigen,TAA,是指一些肿瘤细胞表面糖蛋白或糖脂成分,它们在正常细胞上有微量表达,但在肿瘤细胞表达明显增高。)的scFv和胞内信号域“免疫受体酪氨酸活化基序(immunoreceptortyrosinebasedactivationmotifs,ITAM,通常为CD3ζ或FcεRIγ)”在体外进行基因重组,生成重组质粒,再在体外通过转染技术转染到患者的T细胞,使患者T细胞表达肿瘤抗原受体。转染后经过纯化和大规模扩增后的T细胞,也即CAR-T细胞,可以特异性地识别肿瘤相关抗原,使效应T细胞的靶向性、杀伤活性和持久性较常规应用的免疫细胞大幅提高,并可克服肿瘤局部免疫抑制微环境,从而打破宿主免疫耐受状态,杀灭肿瘤细胞。
完整的CAR-T结构包括抗原结合区、跨膜链接区和胞内信号区三个部分。
CAR-T细胞结构
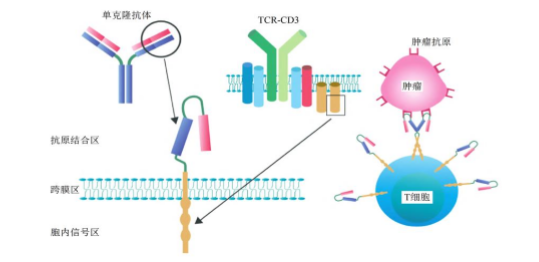
1、四代CAR-T技术演进
研究表明,T细胞的完全活化有赖于双信号和细胞因子的作用。其中第一信号为特异性信号,由TCR识别抗原递呈细胞表面的抗原肽-MHC复合物所启动;第二信号为协同刺激信号,通过CD28/B7等重要的共刺激分子,促进IL-2合成,并使T细胞充分活化及免于凋亡。对于初始型T细胞(未与抗原接触的T细胞),如只在信号1而没有信号2条件下无法使T细胞发挥正常作用;即使T细胞与抗原接触,如果没有协同刺激信号,细胞也不能发挥正常功能。相应的,仅含有CD3ζ序列的嵌合抗原受体,如没有协同刺激信号2,也是无法激活CAR-T细胞。因此,依照T细胞活化的双信号学说,第二和第三代CARs在嵌合受体上加上如CD28、CD134(OX40)和CD137(41BB)等共刺激分子(costimulatorymolecule,CM),增加共同刺激因子的目的是提高T细胞的细胞毒性、增殖活性,维持T细胞应答,延长T细胞存活时间等,从而增强CAR-T的效果。
三代CAR-T胞内信号区变化
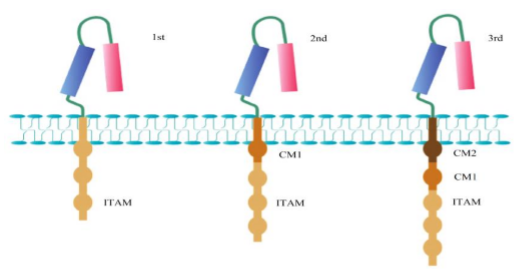
目前已经在开发的第四代CAR-T技术,包括整合表达免疫因子、整合共刺激因子配体等。可以想象,未来还会有更多的共刺激因子以及其他精确调控方式的加入,这也凸显了CAR-T的技术属性。
四代CAR-T技术

2、CAR-T治疗流程
一个典型的CAR-T治疗流程,主要分为以下五个步骤。①分离:从癌症病人身上分离免疫T细胞。②修饰:用基因工程技术给T细胞加入一个能识别肿瘤细胞并且同时激活T细胞的嵌合抗体,也即制备CAR-T细胞。③扩增:体外培养,大量扩增CAR-T细胞。一般一个病人需要几十亿,乃至上百亿个CAR-T细胞(体型越大,需要细胞越多)。④回输:把扩增好的CAR-T细胞回输到病人体内。⑤监控:严密监护病人,尤其是控制前几天身体的剧烈反应。整个疗程持续3个星期左右,其中细胞“提取-修饰-扩增”需要约2个星期,花费时间较长。
CAR-T治疗流程
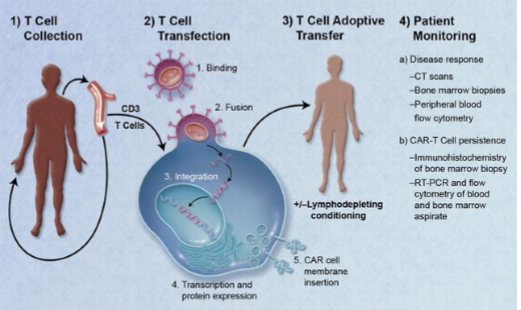
3、CAR-T临床进展
CAR-T疗法是由美国宾夕法尼亚大学终身教授、美国科学院院士CarlJune教授和他的团队首创。后来越来越多的科学家、医院和药企参与到CAR-T技术开发当中。随着不断取得的突破性进展,越来越多的投资机构也看到了这一疗法的前景,资金不断涌入,加速推动了技术进步。
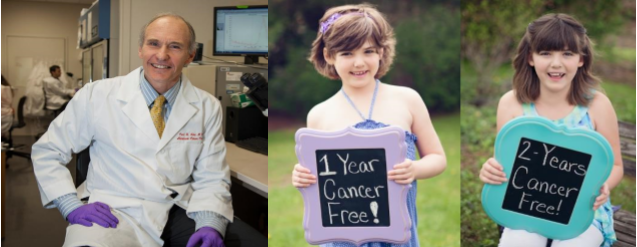
说到CAR-T的临床进展,首先必须要提EmilyWhitehead的故事。5岁时,艾米丽被诊断出急性淋巴细胞白血病,在进行首轮化疗时受到感染,差点失去双腿。后来病情复发,她又接受了治疗,并排期做骨髓移植手术。等待期间,病情再次复发,这时医生们已经无计可施。随后接受CarlJune的CART19细胞回输,Emily的体内发生了超强的免疫反应,连续几天发高烧,不得不入院治疗。高烧下的她产生了幻觉,问爸爸:“我房间里怎么有池塘?”经历了噩梦般的连续高烧后,Emily最终挣脱了死神的束缚重新醒了过来。现在Emily已经9岁,还在健康成长,体内仍然能检测到存活的CAR-T细胞。
CAR-T疗法发明人CarlJune和治愈的EmilyWhitehead
说到CAR-T的临床进展,首先必须要提EmilyWhitehead的故事。5岁时,艾米丽被诊断出急性淋巴细胞白血病,在进行首轮化疗时受到感染,差点失去双腿。后来病情复发,她又接受了治疗,并排期做骨髓移植手术。等待期间,病情再次复发,这时医生们已经无计可施。随后接受CarlJune的CART19细胞回输,Emily的体内发生了超强的免疫反应,连续几天发高烧,不得不入院治疗。高烧下的她产生了幻觉,问爸爸:“我房间里怎么有池塘?”经历了噩梦般的连续高烧后,Emily最终挣脱了死神的束缚重新醒了过来。现在Emily已经9岁,还在健康成长,体内仍然能检测到存活的CAR-T细胞。
CAR-T疗法发明人CarlJune和治愈的EmilyWhitehead

发表在Science上的文章“TheDizzyingJourneytoaNewCancerArsenal”详细的记录了CarlJune和他的团队关于CAR-T临床试验的研发过程。其中关于Emily的部分摘录如下…...EmilyWhitehead,a6-year-oldwithendstageleukemiawhoseparentsturnedtoJune’scelltherapyasalast-ditchhope.Theexperimentaltreatmentsentherbodyintoadeadlyimmuneoverdrive.Shespent2weeksonaventilatorintheCHOPintensivecareunitwhiledoctorstriedeverythingtheycouldthinkoftosaveher.“Wethoughtitwasover,”Junesays.Hedraftedane-mailmessagetoPenn’sprovost:“ItiswithregretthatIinformyouthatourfirstpediatricpatientontheCART19trialwilllikelydie,”hewrote.“Thereisnothingtodoatthispointotherthanhopeforamiracle.”…...(Science.2013.340.1514-1518)
去年以来,几乎每月、甚至每星期都能听到CAR-T临床的新进展以及新技术的开发。现摘取其中一小部分如下。
2014年12月10日,在第56届美国血液学会年会(ASH)上,诺华(Novartis)公布了其CAR-T免疫疗法CTL019的最新临床数据。在这些研究中,CTL019在某些类型淋巴细胞白血病表现出了巨大的治疗潜力。在一项长期儿科研究中,39例复发/难治(r/r)急性淋巴细胞白血病(ALL)儿科患者接受了CTL019的治疗,数据显示,有36例患者经历了完全缓解(CR),比例高达92%(n=36/39)。
2015年5月21日,在英国伦敦举行的第十届世界干细胞与再生医学大会,西比曼(CellularBiomedicineGroup)的首席执行官曹卫公布了其CAR-TCD30霍奇金淋巴瘤免疫-肿瘤研发项目的I期临床数据。7名患者中有5人对CAR-CD30T细胞疗法有应答。该试验由中国解放军总医院设计并执行,项目主要负责人是该院癌症免疫治疗部门的主任韩卫东教授。
2015年6月2日,在美国临床肿瘤学会(ASCO)年会上,纪念斯隆凯特林癌症中心(MSKCC)公布了其CAR-T细胞治疗复发及难治性B细胞型非霍奇金淋巴瘤的临床一期实验结果。8名患者在大剂量化疗和自体造血干细胞移植后接受治疗,其中5名患者完全缓解(62.5%)。部分病人期间经历细胞因子风暴,通过使用tocilizumab联合皮质类固醇治疗得到了有效控制。CarlJune教授在今年接受采访时表示:“CAR-T技术2010年开始做第一次临床实验,估计2017年美国FDA通过,只用7年的时间,这样是很快的。
去年以来,几乎每月、甚至每星期都能听到CAR-T临床的新进展以及新技术的开发。现摘取其中一小部分如下。
2014年12月10日,在第56届美国血液学会年会(ASH)上,诺华(Novartis)公布了其CAR-T免疫疗法CTL019的最新临床数据。在这些研究中,CTL019在某些类型淋巴细胞白血病表现出了巨大的治疗潜力。在一项长期儿科研究中,39例复发/难治(r/r)急性淋巴细胞白血病(ALL)儿科患者接受了CTL019的治疗,数据显示,有36例患者经历了完全缓解(CR),比例高达92%(n=36/39)。
2015年5月21日,在英国伦敦举行的第十届世界干细胞与再生医学大会,西比曼(CellularBiomedicineGroup)的首席执行官曹卫公布了其CAR-TCD30霍奇金淋巴瘤免疫-肿瘤研发项目的I期临床数据。7名患者中有5人对CAR-CD30T细胞疗法有应答。该试验由中国解放军总医院设计并执行,项目主要负责人是该院癌症免疫治疗部门的主任韩卫东教授。
2015年6月2日,在美国临床肿瘤学会(ASCO)年会上,纪念斯隆凯特林癌症中心(MSKCC)公布了其CAR-T细胞治疗复发及难治性B细胞型非霍奇金淋巴瘤的临床一期实验结果。8名患者在大剂量化疗和自体造血干细胞移植后接受治疗,其中5名患者完全缓解(62.5%)。部分病人期间经历细胞因子风暴,通过使用tocilizumab联合皮质类固醇治疗得到了有效控制。CarlJune教授在今年接受采访时表示:“CAR-T技术2010年开始做第一次临床实验,估计2017年美国FDA通过,只用7年的时间,这样是很快的。
本文地址:http://www.zwzyzx.com/show-329-205752-1.html
上一篇:传统过继性免疫细胞治疗
相关资讯
- 国内靶向药物行业监管体制情况(2014-11-13)
- 国内药用辅料在药剂中的作用(2014-11-06)
- 国内药品流通行业分销(商业调拨)批发模式(2015-01-05)
- 我国医疗器械行业主要产业政策(2014-06-04)
- 2014年-2019年我国硝基咪唑类药物市场前景预测(2014-08-07)
- 空间大:国产比例不到10%,进口替代空间巨大(2016-10-25)
- 国内药品流通行业利润水平的变动趋势及变动原因(2015-01-05)
- 国内体外诊断行业主要主管部门(2014-06-11)
合作媒体
最新报告
定制出版
热门报告
免责声明
中为咨询所引述的资料是用于行业市场研究以及讨论和交流,并注明出处,部分内容是由相关机构提供。若有异议请及时联系本公司,我们将立即依据相关法律对文章进行删除或作相应处理。查看详细》》



