去产能之降存量-仿制药一致性评价
相关报告
- 中国化学药品原料药行业市场深度调查研究及投资咨询报告(2018-07-18)
- 全国主要地区特色原料药产业发展状况暨投资环境调查研究报告(2014-11-28)
- 2015-2020年中国环磷酰胺原料药行业运行研究及市场投资发展分析报告(2015-05-08)
- 2014-2018年中国化学药企业拟IPO上市细分市场研究报告(2013-12-10)
- 2016-2022年中国仿制药区域行业市场调查研究及发展分析报告(2015-10-20)
- 2015-2020年中国兽用原料药行业市场主要领域调查分析报告(2015-09-24)
- 2015-2020年中国化学药品原料药行业市场主要领域调查分析报告(2015-09-23)
- 2014版环磷酰胺原料药及其制剂行业企业建设项目可行性研究报告(2014-10-08)
- 2016-2022年中国原料药行业市场深度调查研究及投资咨询报告(2015-11-19)
- 2014-2018年中国仿制药行业市场深度剖析及投资前景趋势研究报告(2014-05-23)
由于受前期的政策审批等因素的制约,国内此前上市的仿制药质量标准较低(如无需采用原研做对照等),再加上国内企业在质量体系、质量控制、工艺技术等方面同国外先进水平有所差距,在某种程度上确实制约了国内仿制药质量水平的提升。
2007之前仿制药审评标准较低
2007之前仿制药审评标准较低

原研药和仿制药的对比举例
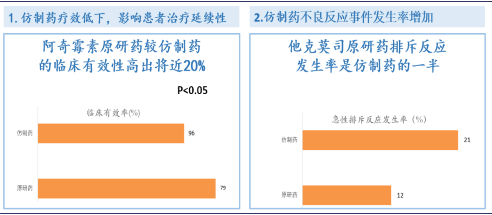
和原研药质量的差异一方面导致了诸多临床不良反应的发生,另一方面也在一定程度上降低了医保资金等医疗资源的使用效率,客观上也促成了外资原研药的“超国民待遇”。也导致了总体上外资原研药的价格普遍比国产仿制药高。此外,根据IMS统计数据显示,在急危重症、疑难病症相对集中的治疗领域,患者对原研药的需求也相对较大。
原研药和国产仿制药应用领域对比
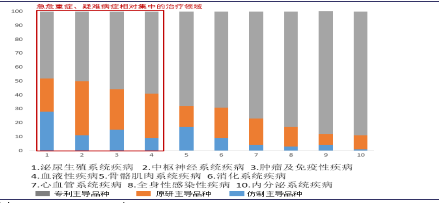
研究报告截止目前口服制剂化药品种批文号接近6万个,国家目前已经颁布了2007年10月1日前的292个基药品种共计19715个文号(含所有剂型、规格),07年以前估计还有上万个批文目录还没公布。08年-15年期间,CFDA批准仿制药生产批文数目超过5000个,这个目录尚未公布,因此可以预估此次受一致性评价影响的文号大约有5万多个,预计几乎国内所有的仿制药企业都会受到影响。
国内外药品质量控制体系

如果说之前制剂企业在手的诸多批文是公司的“财富”的话,那么随着一致性评价的推出,“财富”的“保有成本”将大幅上升,甚至有可能成为企业的“负担”。调查报告从整个行业的角度来看,若2018年化药制剂的一致性评价若能如期完成,则部分企业的“僵尸文号”和“小品种”将大幅减少,多数口服制剂的集中度将会有所提升,从而达到整个仿制药行业去产能和产业升级的目标。
从政策的历史形成来看,一致性评价政策大致可以分成两个阶段,第一个阶段是2012年到2015年上半年,2012年1月20日国务院发布了国家药品安全“十二五”规划,首次提到药品一致性评价的问题,随后虽然发布了一系列政策,但是由于推动的力度不强、相关配套细则未落地等并没有引起充分的重视和落实。第二个阶段是从2015年8月份以来,在医药行业各项政策新政陆续出台的背景下,2016年03月05日,国务院办公厅发布了国办发„2016‟8号《关于开展仿制药质量和疗效一致性评价的意见》,从国务院的层面推动一致性评价陆续进入落实阶段。随后出台的一致性评价的细则越来越多,具体包括如何选择参比制剂、溶出验证原则、人体生物等效豁免品种等核心点基本都浮出水面。
自2012年以来一致性评价的政策演变
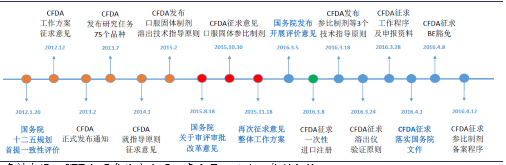
本文地址:http://www.zwzyzx.com/show-329-244788-1.html
相关资讯
- 肿瘤检测市场POCT应用发展情况(2014-06-04)
- 新版GMP 实施促进医药产业升级(2014-10-20)
- 2013年度甘肃地区社区卫生服务中心(站)医疗服务情况分析(2014-04-02)
- 2013年全球主要非甾体抗炎药物市场销售额为251.06亿美元(2014-08-06)
- 我国体外诊断试剂目前主要品种市场份额及趋势(2015-09-06)
- 重庆医药流通业务主要流通区域竞争状况(2015-07-23)
- 制剂新剂型、新工艺的应用推广带来的新型辅料发展机遇(2014-11-06)
- 干细胞的主要简介(2016-11-22)
合作媒体
最新报告
定制出版
热门报告
免责声明
中为咨询所引述的资料是用于行业市场研究以及讨论和交流,并注明出处,部分内容是由相关机构提供。若有异议请及时联系本公司,我们将立即依据相关法律对文章进行删除或作相应处理。查看详细》》



