国内兽药行业主要监管体制情况
相关报告
- 2015-2020年中国禽用疫苗行业市场重点层面调查研究报告(2015-09-24)
- 2014-2018年中国猪用疫苗行业市场深度剖析及投资前景趋势研究报告(2014-09-19)
- 2014-2018年中国动物疫苗行业市场深度剖析及投资前景趋势研究报告(2014-01-09)
- 中国药物饲料添加剂行业市场深度调查研究及投资咨询报告(2018-07-16)
- 2014-2018年禽用疫苗项目商业计划书(2014-10-09)
- 2015-2020年中国细胞毒活苗行业市场发展研究及投资前景分析报告(2015-03-25)
- 2015-2020年中国渔药行业市场重点层面调查研究报告(2015-09-24)
- 2016-2022年中国猪用疫苗行业市场深度调查研究及投资咨询报告(2015-11-19)
- 2014-2018年中国猪用疫苗行业市场深度调查分析及投资战略研究报告(2014-09-19)
- 2016-2022年中国猪用疫苗区域行业市场调查研究及发展分析报告(2015-10-21)
(1)“预防为主”的防疫政策及国家强制免疫制度
《中华人民共和国动物防疫法》提出国家对动物疫病实行―预防为主‖的方针,并对严重危害畜牧业生产和人体健康的动物疫病实施强制免疫。目前,国家对禽流感、高致病性猪蓝耳病、口蹄疫、猪瘟、小反刍兽疫等五种疫病进行强制免疫。随着我国动物疫病防控体系的逐步完善、公共卫生安全的需求和动物疫情的变化,国家还将逐步扩大强制免疫的范围,这将为具有技术创新优势、能够及时研发和生产国家强制免疫用动物疫苗的企业提供巨大的市场机遇。
(2)兽药经营监管体制
根据《兽药管理条例》相关规定,经营兽药的企业必须具备与所经营的兽药相适应的技术人员、仓储设备及质量管理机构等条件,并须获得市、县人民政府兽医行政管理部门颁发的《兽药经营许可证》;经营兽用生物制品的,应当经省、自治区、直辖市人民政府兽医行政管理部门批准并获得颁发的《兽药经营许可证》。
(3)兽药生产许可证制度
根据《兽药管理条例》相关规定,设立兽药企业,必须具有与所生产的兽药相适应的兽药学相关专业技术人员、厂房以及仪器设备等必备条件,并经农业部审查合格后获得《兽药生产许可证》,凭《兽药生产许可证》办理工商登记手续。
《兽药生产许可证》有效期为5年。有效期届满,需要继续生产兽药的,应当在许可证有效期届满前6个月到原发证机关申请换发兽药生产许可证。
(4)兽用生物制品经营监管制度
根据《兽用生物制品经营管理办法》相关规定,兽用生物制品实行分类管理制度,分为国家强制免疫用生物制品和非国家强制免疫用生物制品。国家强制免疫用生物制品名单由农业部确定并公告,并由农业部指定的企业生产,依法实行政府采购,省级人民政府兽医行政管理部门组织分发。农业部指定的生产企业只能将国家强制免疫用生物制品销售给省级人民政府兽医行政管理部门和符合一定要求的养殖场,不得向其他单位和个人销售。兽用生物制品生产企业可以将本企业生产的非国家强制免疫用生物制品直接销售给使用者,也可以委托经销商销售。
(5)新兽药研发和注册制度及产品批准文号制度
《兽药注册办法》规定,新兽药注册申请人应当在完成临床试验后,向农业部提出审批申请,审批合格的,颁发新兽药注册证书。国家对依法获得注册的新兽药在一定时期内实施排他性保护,未取得新兽药注册证书的企业只能生产中国兽药典中同质化的产品。
根据《兽药产品批准文号管理办法》相关规定,兽药企业生产兽药,应当取得农业部核发的产品批准文号。兽药产品批准文号是农业部根据兽药国家标准、生产工艺和生产条件批准特定兽药企业生产特定兽药产品时核发的兽药批准证明文件。
根据《新兽药研制管理办法》、《兽药注册办法》及《兽药产品批准文号管理办法》,新动物疫苗产品的研发和注册、生产前取得产品批准文号的基本程序如下:
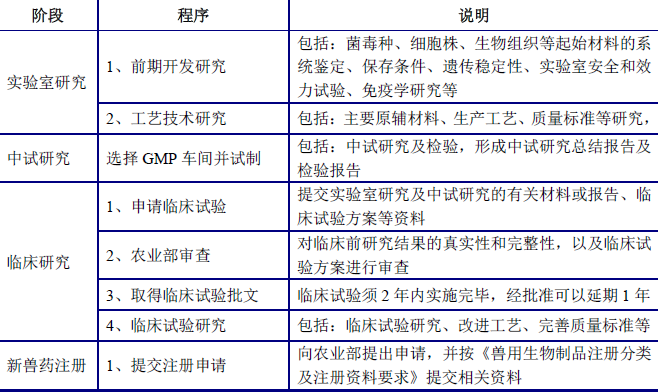

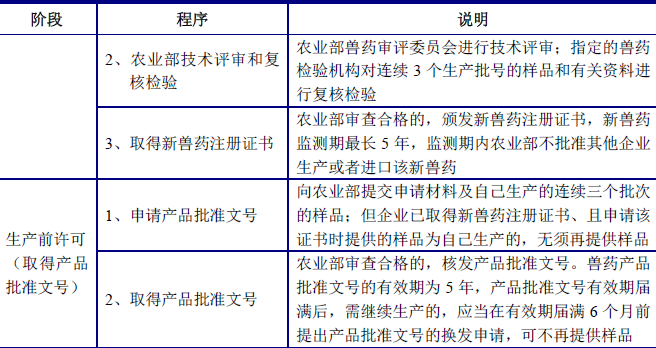
除上述阶段外,基因工程疫苗的研发过程中还需通过农业部的农业转基因生物安全评价。
(6)兽药国家标准制度
根据《兽药管理条例》相关规定,兽药应当符合兽药国家标准。由国家兽药典委员会拟定、农业部发布的《中华人民共和国兽药典》和农业部发布的其他兽药质量标准为国家标准。
(7)质量管理制度
农业部对动物疫苗产品的质量管理制度主要包括:兽药生产质量管理规范(GMP)制度、兽药GMP飞行检查制度和兽用生物制品批签发制度。
兽药生产质量管理规范(GMP)制度:根据《兽药生产质量管理规范》和《实施<兽药GMP规范>的有关要求》的规定,兽药GMP规范自2006年1月1日起强制实施,新开办的兽药企业必须取得兽药GMP证书后方可办理《兽药生产许可证》及产品批准文号;自2006年7月1日起,各地不得经营、使用未取得兽药GMP证书的企业、车间所生产的兽药产品。
兽药GMP飞行检查制度:农业部对已获得GMP证书的企业实行兽药GMP飞行检查制度,在事先不通知被检查企业的情况下,随时对兽药生产企业实施现场检查,核查企业兽药生产质量管理方面的即时状况,以规范兽药生产行为,保证兽药质量。
兽用生物制品批签发制度:中监所对动物疫苗产品在销售前实行批签发制度,未经批签发批准的动物疫苗批次,不得销售。
(8)兽药进出口制度
根据《兽药管理条例》,向中国出口的兽药,出口方应向农业部申请注册,经审查合格后发放进口兽药注册证书。境外企业不得在中国直接销售兽药。为进一步明确对进口兽药的监督管理,农业部制定了《兽药进口管理办法》,规定对进口兽药实行注册管理制度,取得《进口兽药登记许可证》的兽药方能在国内销售、分装、使用;并规定取得《进口兽药登记许可证》的外国企业在中国销售其产品时,必须在中国境内委托合法的兽药经营企业作为其代理商。
本文地址:http://www.zwzyzx.com/show-329-99761-1.html
上一篇:国内动物疫苗行业主要法律法规
下一篇:国内动物疫苗行业主要产业政策情况
相关资讯
- 华韩整形:首家登陆国内资本市场的医美机构,获JCI国际认证(2016-09-12)
- 国内药物行业主管部门、行业监管体制(2015-08-18)
- 韩美代理经销体量小、增速快(2016-06-28)
- 精准医学案例(2016-07-04)
- 医疗的本质由核心供需双方产生(2016-10-08)
- 政策利好社会化办医 迎来医疗服务黄金时代(2016-03-22)
- 医药制造行业具有技术壁垒(2015-12-25)
- 齐全检测菜单可充分满足用户需求(2016-10-25)
合作媒体
最新报告
定制出版
热门报告
免责声明
中为咨询所引述的资料是用于行业市场研究以及讨论和交流,并注明出处,部分内容是由相关机构提供。若有异议请及时联系本公司,我们将立即依据相关法律对文章进行删除或作相应处理。查看详细》》



