国内生物再生材料行业资质管理制度
相关报告
- 数据更新中...
目前,我国对包括生物再生材料在内的医疗器械实行严格的分类管理政策,对医疗器械生产企业实行备案和许可制度,对医疗器械产品生产采取备案和注册制度。根据2014年修订的《医疗器械监督管理条例》,国家对医疗器械按照风险程度分为一类、二类和三类,并实行分类管理,具体如下:
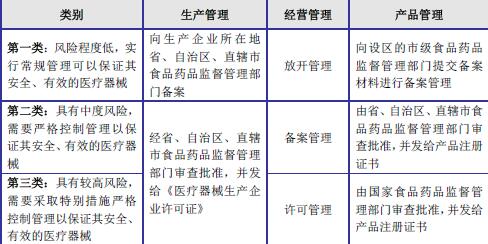
第一类医疗器械实行产品备案管理,第二类、第三类医疗器械实施产品注册管理;第一类医疗器械生产实行备案管理,第二类、第三类医疗器械生产实行审批管理。同时,放开第一类医疗器械的经营,对第二类医疗器械的经营实行备案管理,对第三类医疗器械的经营实行许可管理。
生产的生物再生产品可植入人体用于替代人体部分受损器官,并诱导新组织再生。该等产品的使用直接关系到人体的生命健康,如果产品出现质量问题,具有较高的风险性,因此国家对相关企业的设立、产品的生产与销售资格均进行严格审查,并建立了系统的管理和市场准入制度。根据《医疗器械监督管理条例》、《医疗器械注册管理办法》和《医疗器械经营企业许可证管理办法》的规定,植入性医疗器械的生产和经营需分别取得经省、自治区、直辖市食品药品监督管理部门核发的《医疗器械生产许可证》和设区的市级食品药品监督管理部门核发的《医疗器械经营许可证》,企业生产和销售需取得国家食品药品监督管理部门的前置许可。此外,企业产品研发完成后在生产经营前需取得国家食品药品监督管理总局颁发的《医疗器械注册证》,只有取得《医疗器械注册证》的产品才能上市销售。
本文地址:http://www.zwzyzx.com/show-262-190149-1.html
上一篇:国内生物再生材料主要产业政策情况
下一篇:生物再生材料的概念
相关资讯
- 南京医药(600713):致力业务创新的国企改革先锋(2016-09-09)
- 妊娠检测市场POCT应用发展情况(2014-06-04)
- 国内医疗器械及服务行业主管部门(2015-07-17)
- 全球兽药主要出口国的相关规定(2015-06-21)
- 美国:国家投资推动,区域医疗卫生信息组织运营(2016-03-21)
- 医药流通行业利润水平的变动趋势及变动原因(2014-08-18)
- 士卓曼:全球种植牙领先企业,向全方案解决者转型进发(2016-10-25)
- 体外诊断产品大型服务商可以为制造商提供延伸服务(2015-05-14)
合作媒体
最新报告
定制出版
热门报告
免责声明
中为咨询所引述的资料是用于行业市场研究以及讨论和交流,并注明出处,部分内容是由相关机构提供。若有异议请及时联系本公司,我们将立即依据相关法律对文章进行删除或作相应处理。查看详细》》



