研发驱动型小型biotech药企-2.0模式
相关报告
- 2014-2018年中国抗微生物药企业拟IPO上市细分市场研究报告(2014-10-08)
- 2015-2020年中国生物药品行业市场重点层面调查研究报告(2015-09-23)
- 2018-2022年中国抗肿瘤药物行业市场深度调查研究及投资咨询报告(2017-10-31)
- 2014-2018年中国抗微生物药行业市场深度剖析及投资前景趋势研究报告(2014-09-12)
- 2014-2018年化学药项目商业计划书(2013-12-11)
- 2016-2022年中国生物药品区域行业市场调查研究及发展分析报告(2015-10-21)
- 2014版抗微生物药行业企业建设项目可行性研究报告(2014-10-09)
- 中国抗微生物药行业市场深度调查研究及投资咨询报告(2018-07-17)
- 2014-2018年中国兽用化学药行业市场深度调查研究及投资前景分析报告(2014-09-19)
- 中国抗肿瘤药行业市场深度调查研究及投资咨询报告(2018-07-18)
过去的十年,我们已经习惯于独家大品种,习惯于“中国神药”,以至于忽略了在中国还有一批致力于新药研发的创新型企业。在行业政策面临巨变的今天,我们也不应只看到行业增速的下降,更要看到巨变中蕴藏着的创新机遇。类似于百济神州、复旦张江、信达生物、君实生物这样的小型研发型药企有望在未来的竞争中一枝独秀。
1、信达生物
信达生物是一家致力于高端生物药制药公司。信达生物公司建立起了一条包括10个新药品种的产品链,覆盖肿瘤、眼底病、自身免疫疾病、心血管病等四大疾病领域,其中两个品种入选国家“重大新药创制”专项,建成了大规模的产业化基地。
2015年3月,礼来和信达将联合开发至少3种潜在治疗淋巴瘤、胃癌、肺癌等多种肿瘤的药物。其中,礼来将提供其cMET单克隆抗体项目,用于开发非小细胞肺癌的治疗,信达将提供以CD20为靶点的单抗药物和一个临床前试验药物进行合作。研发工作将由信达完成,礼来负责将其成功研发出来的产品商业化。这个项目礼来出价4亿美元,这使得信达的产品可以在研发完成后就可快速进入国际市场获得回报。随后在恒瑞医药将其PD-1抗体出售后的一个月后,即2015年10月,礼来跟信达又达成协议将出价10亿美元跟信达共同研发信达的3个PD-1药物。
信达临床受理与注册列表
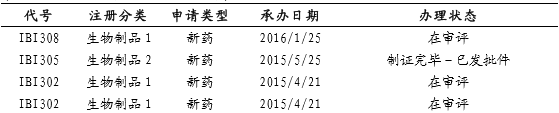
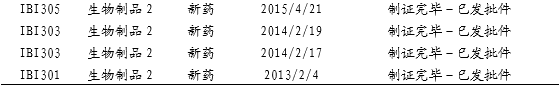
信达临床试验项目列表

2、百济神州
百济神州成立于2011年1月24日,是一家全球性的、以研发为基础的生物科技公司,目前有超过200名科学家,临床医学家和员工。公司专注于开发和推广靶向和免疫肿瘤治疗,在研产品线包括新型小分子口服靶向类和单克隆抗体类抗癌药物,并已有部分产品进入临床试验阶段。百济神州致力于通过寻找最优的肿瘤药物联合治疗方案,使癌症患者的生存质量和生存期获得显著提高。百济神州的ADS股票在美国纳斯达克证券交易所GlobalSelectMarket板块进行交易,代码为“BGNE”。
公司在早期就开发了一个癌症生物学平台,以提供更好的药物研究模型和流程。通过与国内领先的肿瘤中心建立密切联系,可获得大量肿瘤活检标本和组织样本,构建新的体内、体外和细胞生物学水平肿瘤模型,从而更好地选择靶点,并筛选和评估可能具有显著单一或组合疗效潜力的药剂。目前公司有4个药物进入临床,3个小分子药物BGB-3111、BGB-283、BGB-290和一个单抗药物BGB-A317。
百济神州在研药物管线
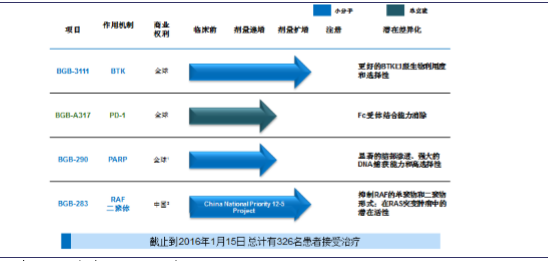
此外,肿瘤免疫制剂与靶向疗法结合有可能产生协同作用,形成更持久的抗肿瘤反应,并提高肿瘤患者生存率。目前公司正在开发的肿瘤免疫试剂BGB-A317以及三种靶向疗法,包括BGB-3111、BGB-290以及BGB-283有望在组合治疗中大展头角,BGB-A317+BGB-3111、BGB-A317+BGB-290、BGB-A317+BGB-283的三种组合在小鼠癌症治疗模型及其他类似模型中均表现一定的抑制协同作用。
百济神州肿瘤免疫和靶向组合疗法
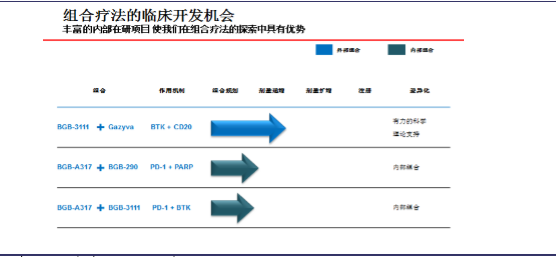
本文地址:http://www.zwzyzx.com/show-262-238415-1.html
相关资讯
- 国家政策的支持医用敷料的发展(2015-12-29)
- 体外诊断试剂监督管理方面的法律法规(2014-06-25)
- 人体微量元素检测产品行业与上下游行业之间的关联性及影响(2015-08-25)
- 2013年度陕西地区医疗卫生人员规模情况(2014-03-31)
- 体外诊断行业周期性、区域性特征(2014-06-25)
- 2003-2012年全国医疗机构数量规模情况(2014-03-31)
- 全球医药市场继续保持快速增长态势(2014-07-14)
- 丙肝:第二大肝病介绍(2016-06-23)
合作媒体
最新报告
定制出版
热门报告
免责声明
中为咨询所引述的资料是用于行业市场研究以及讨论和交流,并注明出处,部分内容是由相关机构提供。若有异议请及时联系本公司,我们将立即依据相关法律对文章进行删除或作相应处理。查看详细》》



