针对新药开启史上最严临床数据核查,影响企业未来现金流预期
相关报告
- 2014-2018年中国仿制药业兼并重组及投资建议研究分析报告(2014-09-30)
- 2014版化学药行业企业建设项目可行性研究报告(2014-10-08)
- 2014-2018年中国中成药生产行业兼并重组及投资建议研究报告(2013-12-08)
- 2015-2020年中国化学药行业市场主要领域调查分析报告(2015-09-23)
- 2014-2018年中国中成药行业市场发展研究及投资咨询研究报告(2014-01-04)
- 2014-2018年中国兽用化学药行业市场深度调查研究及投资前景分析报告(2014-09-19)
- 2015-2020年中国仿制药行业运行研究及市场投资发展分析报告(2015-05-07)
- 2014-2018年化学药品项目商业计划书(2014-10-09)
- 2014-2018年中国化学药品企业拟IPO上市细分市场研究报告(2014-10-09)
- 中国化学药品原料药行业市场深度调查研究及投资咨询报告(2018-07-18)
针对新药品种,食药监总局开启了一轮史上最严格的临床数据核查。2015年8月国务院发布《关于改革药品医疗器械审评审批制度的意见》,着重强调了要提高我国药品审批标准。和《意见》大约同时期,国家食药监总局发布了《关于开展药物临床试验数据自查核查工作的公告》。《公告》强调,为从源头上保障药品安全、有效,国家食品药品监督管理总局决定,对已申报生产或进口的待审药品注册申请开展药物临床试验数据核查,以着力解决我国一部分“新药”临床质量不高、数据部分造假、注册申请积压等一系列问题。
“史上最严”核查导致大量排队注册申请撤回,直接影响企业的未来现金流预期。此轮核查的严格程度超过了此前市场的预期。2015年底,CFDA公布了两轮抽查的审查结果,对于抽检的11个企业的24个药品注册申请,临床试验数据全部有问题,不予批准相关注册。抽查中的100%拒绝率吓退了整个行业,绝大多数企业陆续撤回了新药注册申请。《关于开展药物临床试验数据自查核查工作的公告》发布时,排队注册申请的共有1622个药品品种,而根据CFDA网站公告总结,研究报告截止目前1622个品种中,除去193个不需要临床试验的药品品种,共有1171个品种撤回,占比高达81.9%。研发一个新药的投入成本非常高,市场分析根据新康界的统计,近三年来新药研究成本的交易价格通常在3000万元以上,一些医药专家的估算更高,认为中国研发一个新药平均成本在2亿元左右。因此,市场对于一些研发接近尾声、申请获批等待生产的药企有着较为乐观的未来预期,如果申请被拒或主动撤回,都会对现金流预期带来较大负面影响,对于没有实质研发能力的企业无疑是巨大冲击。
2013-2014年中国新药研究成果交易样本情况


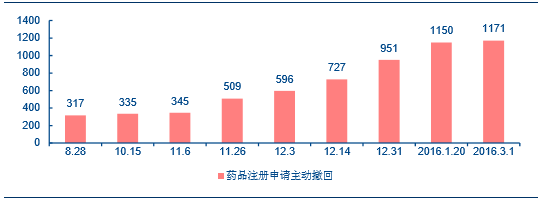
开展临床试验后主动申请撤回的药品品种愈发增多
本文地址:http://www.zwzyzx.com/show-262-245522-1.html
相关资讯
- 医药行业的周期性、区域性和季节性特征(2015-05-25)
- 国内创新药新机遇—药政改革(2016-07-15)
- 东洋BK医院:全韩第一家整形医院,根基深厚(2016-09-12)
- 国内与中药行业相关的法律法规和产业政策(2015-05-14)
- 城市水环境服务市场需求情况(2015-05-15)
- 2013年度云南地区医疗卫生机构数量规模情况(2014-03-31)
- 体制外传统诊所的发展困境(2016-08-22)
- 慢性疼痛的基因治疗(2016-11-22)
合作媒体
最新报告
定制出版
热门报告
免责声明
中为咨询所引述的资料是用于行业市场研究以及讨论和交流,并注明出处,部分内容是由相关机构提供。若有异议请及时联系本公司,我们将立即依据相关法律对文章进行删除或作相应处理。查看详细》》



