国内医药外包服务主要相关法律法规
相关报告
- 数据更新中...
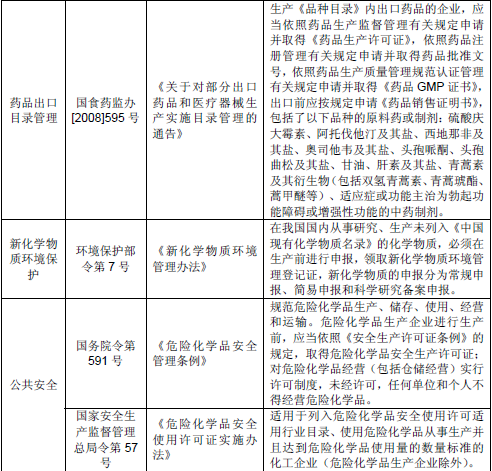
(1)国内主要相关法律法规
②ICH国际协调会议要求

(2)出口地主要法律法规
①药品法典要求
包括了CFR(CodeofFederalRegulations)美国《联邦规章典籍》第21章“食品与药品”的相关规定以及《欧洲药典》第七版。此外,欧洲议会和欧盟理事会要求从2013年7月开始,所有出口到欧盟的原料药均需出具出口国监管部门的书面声明,以符合欧盟监管要求。
②ICH国际协调会议要求
为了严格管理药品质量,必须对药品的研制、开发、生产、销售等进行控制和审批,从而形成了药品注册制度。但是由于不同国家对药品注册的要求各不相同,这不利于病人在药品安全性、有效性和质量方面得到科学的保证,同时也阻碍了医药事业的发展。1990年由美国、日本和欧盟三方的政府药品注册部门和制药行业共同发起了ICH即人用药物注册技术要求国际协调会议。其推出的ICHQ7已经成为全球原料药生产的共同指南。
本文地址:http://www.zwzyzx.com/show-329-124564-1.html
下一篇:国家医药外包服务主要产业政策
相关资讯
- 2013年度甘肃地区各类医疗卫生机构床位数分析(2014-04-01)
- 2012-2013年全国卫生行业固定资产投资施工、投产项目数情况(2014-02-12)
- 国内医药流通行业主要政策情况(2014-12-10)
- 近10年来新药分子结构已越来越复杂(2015-04-08)
- 2013年度西藏地区乡镇卫生院医疗服务情况分析(2014-04-02)
- 灯盏花素、灯盏花乙素的疗效、药理基础和应用范围(2015-04-08)
- 全球骨科医疗器械市场构成情况(2015-08-24)
- 新博林(利巴韦林颗粒)在利巴韦林颗粒剂中的市场地位(2014-07-14)
合作媒体
最新报告
定制出版
热门报告
免责声明
中为咨询所引述的资料是用于行业市场研究以及讨论和交流,并注明出处,部分内容是由相关机构提供。若有异议请及时联系本公司,我们将立即依据相关法律对文章进行删除或作相应处理。查看详细》》



