医疗器械行业监管体制
相关报告
- 2016-2022年中国血液净化类产品区域行业市场调查研究及发展分析报告(2015-10-22)
- 2015-2020年中国留置导管行业运行研究及市场投资发展分析报告(2015-05-12)
- 2016-2022年中国注射类产品行业市场深度调查研究及投资咨询报告(2015-11-20)
- 2016-2022年中国输液输血类产品区域行业市场调查研究及发展分析报告(2015-10-22)
- 中国血液净化类产品行业市场深度调查研究及投资咨询报告(2018-07-19)
- 2015-2020年中国留置导管行业深度调研及市场投资发展研究报告(2015-06-27)
- 2015-2020年中国输液输血类产品行业运行研究及市场投资发展分析报告(2015-05-12)
- 2015-2020年中国注射类产品行业深度调研及市场投资发展研究报告(2015-06-27)
- 2015-2020年中国一次性医疗器械行业市场深度剖析及投资发展研究报告(2015-06-27)
- 2016-2022年中国输液输血类产品行业市场深度调查研究及投资咨询报告(2015-11-20)
(1)国家对医疗器械实行分类管理
国家对医疗器械按照风险程度实行分类管理:

(2)国家对医疗器械产品实行注册与备案制度
我国对第Ⅰ类医疗器械实行产品备案管理,对第Ⅱ类、第Ⅲ类医疗器械实行产品注册管理。

受理注册申请的食品药品监督管理部门对符合安全、有效要求的医疗器械应准予注册并发给医疗器械注册证。医疗器械注册证书有效期5年,有效期届满需要延续注册的,应当在有效期届满6个月前提出延续注册的申请。除存在不予延续注册的情形外,相关食品药品监督管理部门应当在医疗器械注册证有效期届满前作出准予延续的决定,逾期未作出决定的,视为准予延续。
(3)国家对医疗器械生产企业实施分类管理
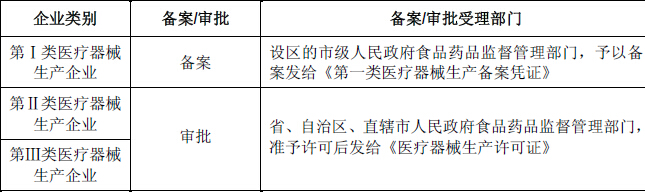
医疗器械生产许可证有效期为5年。有效期届满需要延续的,依照有关行政许可的法律规定办理延续手续。
(4)国家对医疗器械经营企业实施分类管理
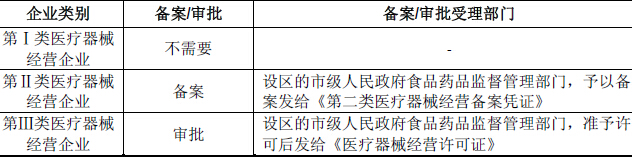
医疗器械经营许可证有效期为5年。有效期届满需要延续的,依照有关行政许可的法律规定办理延续手续。
本文地址:http://www.zwzyzx.com/show-329-133163-1.html
下一篇:医疗器械行业主要法律法规
相关资讯
- 植物提取物行业市场规模分析(2016-06-24)
- 国内多肽药物市场——未来发展空间巨大(2016-05-16)
- 体外诊断行业市场需求现状(2016-06-24)
- 我国落实禁烟通知的政策措施研究分析(2014-01-13)
- 重点公司产品分析:Dexcom德康医疗G4(2016-05-13)
- 产业链明确:国内企业集中基因测序与检测服务(2016-09-14)
- 医药流通上下游行业资源的积累壁垒情况(2014-08-18)
- 大容量注射剂主要竞争对手市场份额(2015-07-23)
合作媒体
最新报告
定制出版
热门报告
免责声明
中为咨询所引述的资料是用于行业市场研究以及讨论和交流,并注明出处,部分内容是由相关机构提供。若有异议请及时联系本公司,我们将立即依据相关法律对文章进行删除或作相应处理。查看详细》》



