化药注册分类改革重新定义创新药的概念
相关报告
- 2014版抗肿瘤药行业企业建设项目可行性研究报告(2014-10-09)
- 全国主要地区抗肿瘤药产业发展状况暨投资环境调查研究报告(2014-11-28)
- 2015-2020年中国抗肿瘤药物行业市场主要领域调查分析报告(2015-09-23)
- 2014-2018年抗微生物药项目商业计划书(2014-10-09)
- 2015-2020年中国化学药品制剂行业市场主要领域调查分析报告(2015-09-24)
- 2014版抗微生物药行业企业建设项目可行性研究报告(2014-10-09)
- 2013-2014年全国化学药行业调查报告暨产业链研究报告(2014-05-23)
- 2014-2018年中国抗肿瘤药行业市场深度调查研究及投资前景分析报告(2014-09-12)
- 2015-2020年中国抗微生物药行业市场深度剖析及投资发展研究报告(2015-06-25)
- 2016-2022年中国生物药品区域行业市场调查研究及发展分析报告(2015-10-21)
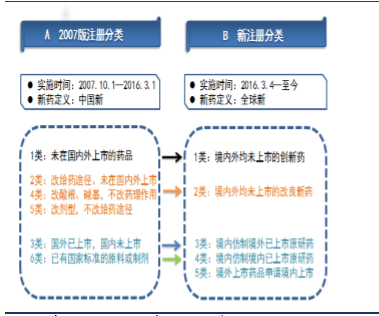
为鼓励新药创制,严格审评审批,提高药品质量,促进产业升级,CFDA于2016年3月发布了《化学药品注册分类改革工作方案》,对当前化学药品注册分类进行改革。新版方案对新药的定义从“中国新”提升至“全球新”,新药必须是境内外均未上市的药品,并进一步分为1类新药(创新药)和2类新药(改良型新药)。新注册分类1为创新药,强调是含有新的结构明确的、具有药理作用的化合物,且具有临床价值的原料药及其制剂,不包括改良型新药中2.1类的药品;新注册分类2为改良型新药,强调“优效性”,即相较于被改良的药品,具备明显的临床优势,基本堵死了以前流行的低水平改剂型、给药途径、改酸根碱基成酯类“新药”的路,再考虑到原研厂家严密的专利保护体系,今后在具备临床优势的前提下开发改良型新药的难度未必小于1类新药,行业调查报告所以我们预计今后在新药研发过程中,临床价值评估变得越来越重要;新注册分类3为仿制境外上市但境内未上市原研药品的药品,大致相当于原有分类中的3类新药,在此次注册分类变革中受到的冲击最大,在新的分类中被纳入仿制药的行列,此外,新药监测期被取消,以前部分首仿品种通过“新药监测期+招标档期”长期和原研共分市场的情形将很难再现,首仿品种的价值将被大大削弱。
新旧化药注册分类对应
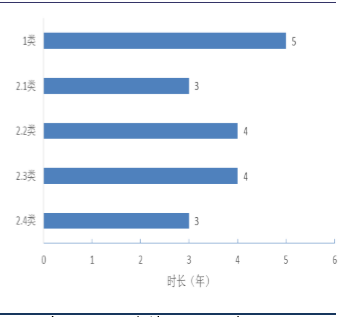
新注册分类下的新药监测期
本文地址:http://www.zwzyzx.com/show-329-238375-1.html
上一篇:创新药审批加速
相关资讯
- 中成药行业与上下游行业关联及影响情况(2014-06-07)
- 国内医药流通市场集中度进一步上升(2014-08-18)
- 中国医美消费群体不同收入占比情况(2016-03-21)
- CTC、ctDNA和外泌体是液态活检的“三驾马车”(2016-08-11)
- 我国心脑血管疾病患病率情况(2015-05-15)
- 2013年度安徽地区各类医疗卫生机构床位数分析(2014-04-01)
- 国内医药行业的技术水平和技术特点(2014-09-18)
- 城市公立医院化学药用药市场TOP20产品市场份额(2016-03-22)
合作媒体
最新报告
定制出版
热门报告
免责声明
中为咨询所引述的资料是用于行业市场研究以及讨论和交流,并注明出处,部分内容是由相关机构提供。若有异议请及时联系本公司,我们将立即依据相关法律对文章进行删除或作相应处理。查看详细》》



