制剂出口企业转内销机会:华海药业
相关报告
- 2015-2020年中国特色原料药行业市场深度剖析及投资发展研究报告(2015-06-25)
- 2014版医药行业企业建设项目可行性研究报告(2013-12-11)
- 2016-2022年中国原料药行业市场深度调查研究及投资咨询报告(2015-11-19)
- 2014-2018年中国仿制药行业市场深度调查研究及投资前景分析报告(2014-05-23)
- 2014-2018年中国原料药企业拟IPO上市细分市场研究报告(2014-10-08)
- 中国制剂仿制药行业市场深度调查研究及投资咨询报告(2018-07-17)
- 2015-2020年中国中成药制剂行业市场深度剖析及投资发展研究报告(2015-06-26)
- 2014-2018年中国中成药制剂行业市场深度调查研究及投资前景分析报告(2014-09-25)
- 2014-2018年中国化学原料药企业拟IPO上市细分市场研究报告(2014-10-08)
- 2015-2020年中国中成药行业市场深度剖析及投资发展研究报告(2015-06-25)
公司作为优质仿制药企业的代表,中长期有望率先受益。截止2015年底,公司合计拥有20个美国FDA批准的ANDA批文,其中有8个品种目前已经在国内上市。研究报告未来公司可以利用前述第一条规则(在中国境内用同一条生产线生产上市并在欧盟、美国和日本获准上市的药品,经CFDA资料审核及生产现场进行检查后视同通过一致性评价),推动这几个品种率先、快速通过一致性评价。如其他企业未能及时跟进,华海药业则有机会充分占领市场。
华海药业可以通过一致性评价规则实现“出口转内销”
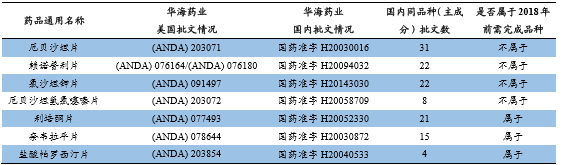
此外,市场分析根据第二条优惠条款,制剂出口企业可以将海外上市的仿制药拿回国内走5.2类审批通道,实现快速上市,并且可以同时被认定为通过一致性评价。以华海药业为例,目前共有12个品种符合该条款,其中11个品种不属于强制性完成品种,意味着华海药业拥有抢占市场的机会。
华海药业可以通过5.2实现海外仿制品种的快速上市并占领市场
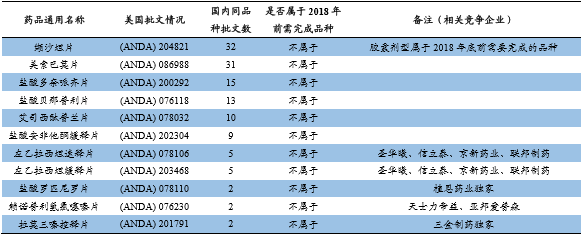
本文地址:http://www.zwzyzx.com/show-329-243376-1.html
上一篇:CRO行业:综合业务能力是关键
相关资讯
- 2006-2012年全国新型农村合作医疗当年基金支出情况分析(2014-04-03)
- 精准医学计划的短期目标和长期目标(2016-07-04)
- 国内人体微量元素检测产品行业发展的不利因素(2015-08-25)
- 国内体外诊断产品行业主要产业政策(2014-06-25)
- 苄达赖氨酸滴眼液药理学分析(2014-12-27)
- 药用空心胶囊行业的上游行业主要是明胶行业(2014-08-19)
- 益丰药房——收入快速增长、净利率逐年提升(2016-05-27)
- 中国中药注射剂行业发展情况(2016-01-27)
合作媒体
最新报告
定制出版
热门报告
免责声明
中为咨询所引述的资料是用于行业市场研究以及讨论和交流,并注明出处,部分内容是由相关机构提供。若有异议请及时联系本公司,我们将立即依据相关法律对文章进行删除或作相应处理。查看详细》》



