国内体外诊断试剂行业监管体制情况
相关报告
- 2014-2018年中国生物制品行业市场深度调查研究及投资前景分析报告(2014-06-13)
- 2015-2020年中国生物制药行业市场深度剖析及投资发展研究报告(2015-06-26)
- 2014-2018年中国生物制品业兼并重组及投资建议研究分析报告(2014-10-08)
- 2015-2020年中国分子诊断试剂行业市场重点层面调查研究报告(2015-09-24)
- 全国主要地区肿瘤类生物制品产业发展状况暨投资环境调查研究报告(2014-12-01)
- 2016-2022年中国体外诊断试剂行业市场深度调查研究及投资咨询报告(2015-11-19)
- 全国主要地区诊断用生物制品产业发展状况暨投资环境调查研究报告(2014-11-28)
- 2014-2018年中国抗毒素类生物制品业兼并重组及投资建议研究分析报告(2014-10-09)
- 2014版生化诊断试剂行业企业建设项目可行性研究报告(2014-10-09)
- 2014版病毒立克次氏体类生物制品行业企业建设项目可行性研究报告(2014-10-09)
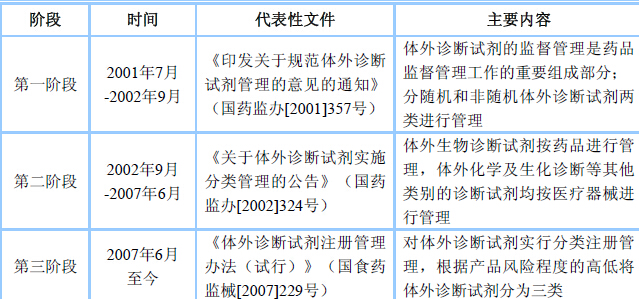
我国体外诊断试剂行业的监管体制先后经历了三个阶段,由最初作为药品进行监督管理的模式,到作为药品和医疗器械相结合的监督管理体制,发展到目前把体外诊断试剂作为单独一类产品进行管理。三个阶段的具体情况如下表所示:
本文地址:http://www.zwzyzx.com/show-348-112570-1.html
上一篇:国内体外诊断试剂行业主管部门
相关资讯
- 我国工业能效管理管理行业主要竞争对手(2014-06-01)
- 国内供应链管理行业重点企业介绍(2016-03-08)
- 国内整合营销传播服务行业内主要企业情况(2015-07-24)
- 生猪分类情况介绍(2015-07-31)
- 连接器与屏蔽罩供应商与客户之间形成联动的开发机制(2014-06-30)
- 国内矿山管理行业与其上、下游行业的关系(2014-12-18)
- 目前国内广告业中的主要法律法规(2014-06-18)
- 影响我国园艺用品行业发展的有利因素(2014-06-12)
合作媒体
最新报告
定制出版
热门报告
免责声明
中为咨询所引述的资料是用于行业市场研究以及讨论和交流,并注明出处,部分内容是由相关机构提供。若有异议请及时联系本公司,我们将立即依据相关法律对文章进行删除或作相应处理。查看详细》》



