中国体外诊断产品行业主要法律法规
相关报告
- 中国重组抗原疫苗行业市场深度调查研究及投资咨询报告(2018-07-19)
- 2016-2022年中国细菌类诊断抗原行业市场深度调查研究及投资咨询报告(2015-11-19)
- 2014版荧光抗体行业企业建设项目可行性研究报告(2014-10-09)
- 2015-2020年中国单克隆抗体制剂行业市场调查研究及投资发展分析报告(2015-05-12)
- 2015-2020年中国体外诊断产品行业市场重点层面调查研究报告(2015-09-25)
- 全国主要地区诊断用单克隆抗体产业发展状况暨投资环境调查研究报告(2014-12-01)
- 2014版毒素类诊断抗原行业企业建设项目可行性研究报告(2014-10-09)
- 2014版梅毒诊断抗原行业企业建设项目可行性研究报告(2014-10-09)
- 中国诊断用单克隆抗体行业市场深度调查研究及投资咨询报告(2018-07-18)
- 中国体外诊断产品行业市场深度调查研究及投资咨询报告(2018-07-20)
体外诊断试剂行业相关主要法律法规和规章如下:
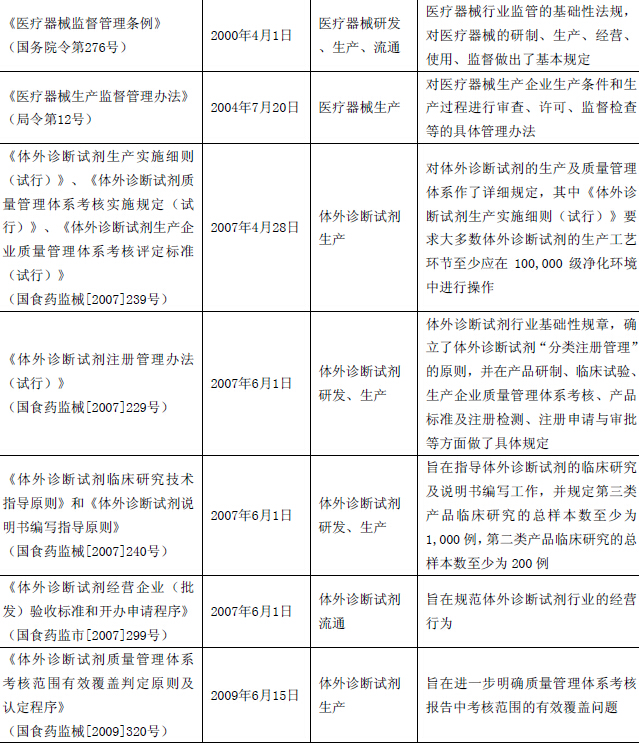
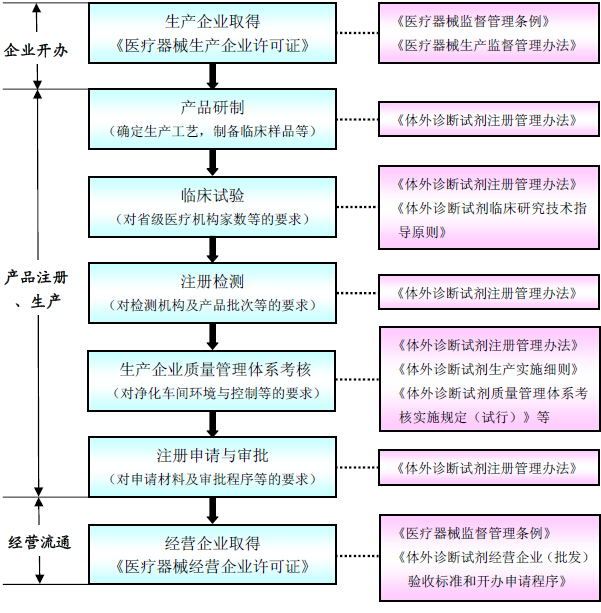
下图为体外诊断试剂企业从开办到产品注册、生产、经营各阶段法规的要求:

本文地址:http://www.zwzyzx.com/show-262-170677-1.html
上一篇:中国体外诊断产品行业监管体制
下一篇:中国体外诊断产品主要行业政策
相关资讯
- 国内医用导管市场容量和未来趋势(2015-01-28)
- 医药制造业的周期性、区域性或季节性特征(2014-06-22)
- 样本医院用药金额主要大类份额变化情况(2015-05-15)
- 牙科连锁趋势:医师资源、高附加值项目、目标定位为核心竞争力(2016-10-25)
- 乐普基因:公司的产品包括检测服务和分子诊断试剂两类(2016-08-26)
- 多家企业通过WHO预认证,积极布局国际市场(2016-03-23)
- 国内医疗器械行业监管体制(2016-01-20)
- 迈克生物(300463):化学发光持续放量,持续向IVD龙头迈进(2016-10-25)
合作媒体
最新报告
定制出版
热门报告
免责声明
中为咨询所引述的资料是用于行业市场研究以及讨论和交流,并注明出处,部分内容是由相关机构提供。若有异议请及时联系本公司,我们将立即依据相关法律对文章进行删除或作相应处理。查看详细》》



