我国新药研发环境显著改善,创新药研发如火如荼
相关报告
- 2015-2020年中国抗肿瘤药物行业市场重点层面调查研究报告(2015-09-23)
- 2015-2020年中国化学药品制剂行业市场重点层面调查研究报告(2015-09-24)
- 2015-2020年中国生物药品行业市场重点层面调查研究报告(2015-09-23)
- 2015-2020年中国兽用化学药行业市场主要领域调查分析报告(2015-09-24)
- 2014-2018年中国兽用化学药行业市场深度调查分析及投资战略研究报告(2014-09-19)
- 2014-2018年中国化学药行业市场全面深度调查研究及投资研究报告(2013-12-29)
- 2016-2022年中国抗肿瘤药区域行业市场调查研究及发展分析报告(2015-10-21)
- 2015-2020年中国抗微生物药行业深度调研及市场投资发展研究报告(2015-06-25)
- 2015-2020年中国抗微生物药行业市场调查研究及投资发展分析报告(2015-05-09)
- 2014-2018年中国抗肿瘤药行业市场深度剖析及投资前景趋势研究报告(2014-09-12)
创新药物是医药领域利润最丰厚,也是最能体现技术含量的部分,未来这一领域是最能维持高利润水平的领域。从长远来看,创新药物的研发能力仍然是企业的核心竞争力所在。新药的研发要经历化合物筛选、临床前试验、临床试验、注册申报等过程,从整个研发历程来看,创新药的研发难度都是极其大的,5000-10000个候选化合物才能有一个药物最终上市,一个创新药研发周期耗时长达10年,平均每个创新药的研发费用达到数十亿美金,所以创新药的研发需要巨大的资金投入和强大的研发实力作为支撑。
创新药研发历程
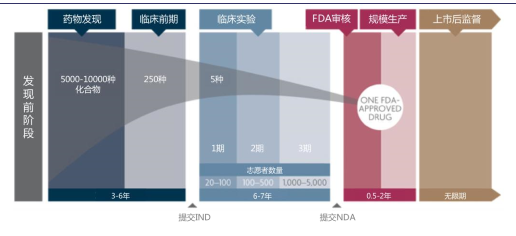
以国外创新药巨头强生为例,行业调查报告2002-2012年间共上市新药13个,累计研发投入676.2亿美元,平均每个新药的研发成本为52.0亿美元;国内创新药研发成本肯定比国外低很多,以恒瑞医药的艾瑞昔布为例,研发成本约1-2亿元,即便如此,由国内化学药上市公司的盈利水平和研发投入情况来看,也只有中国生物制药、恒瑞医药等极少数企业才有能力持续投入较大规模的研发费用。
国内主要制药企业近几年的研发表现
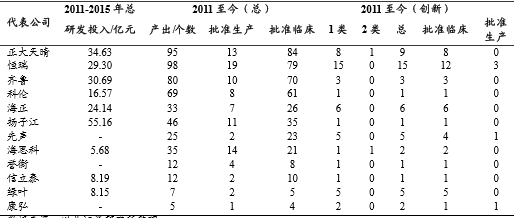
根据美国FDA的规定,创新药物包括以下四类:药品中含有新化学体(NCE)作为该药的活性成分;药品含已有的活性成分但这个成分在美国从未作为医学用过(也称NCE);药品先前已被FDA批准上市,但现在建议新的用法、适应症;药品先前已被批准上市,但现在建议的剂型、给药途径或其他重要条件不同于先前批准的药品,这个也包括RxtoOTC。目前创新药物的主要研发方向有:1)创制新颖的分子结构类型“NCE/NME”—突破性创新药物研究开发。2)创制“me-too”新药—模仿性创新药物研究开发。3)已知药物的进一步研究开发—延伸性创新药物研究开发。4)现有药物的药剂学研究开发—发展制剂新产品。5)应用现代新技术对老产品的生产工艺进行重大的技术革新和技术改造。
中为认为中国的创新药研发可以分四步走,首先从“仿制”转型为“创新”,即从研制“me-too”做起,如恒瑞医药的艾瑞昔布是“me-too”类药物;第二步是“me-better”,围绕原NCE结构基础上进行二次创新,虽然有结构上仿的特点,但更有创造其自身独特优势的地方,素有“国产易瑞沙”之称的浙江贝达药业的埃克替尼、抗肿瘤作用优于同类药物PTK787(诺华和德国先灵联合研发)的恒瑞医药的阿帕替尼都属于此类药物;第三步是“best-in-class”(BIC),是“me-better”里更强的一个,例如Pfizer的万艾可,也是一些系列化合物同时发现,但最终只用一个化合物成药,这个药物选择,对Pfizer当时就是BIC,到后来竞争激烈,其他类似药物被开发,并且突破Pfizer专利,就是metoo和mebetter了;第四步就是“first-in-class”(FIC)药物,即全新化合物,同时靶点也是新的,此类药物研发风险极高,但成功者也是有不少,获得诺贝尔奖的青蒿素就属于此类。
从长期计议,全新创新(first-in-class)类创新药物的研发是我国从医药大国转变为医药强国的重要途径。我国创新的层次主要处于以仿制为主到仿创结合的阶段,仿制药占比达到96%,上市药物多为me-too药物,新药市场被国际大公司产品垄断,缺乏首创药物(first-in-class)。对国内企业而言,结合当前国内临床需求,在国际新药产品基础上开发药效和安全性相似的药物(me-too),或更好的新药(me-better)是目前比较切实可行的创新路径,也是国内创新药研发的主流方向。
热门靶点的创新药申报数量
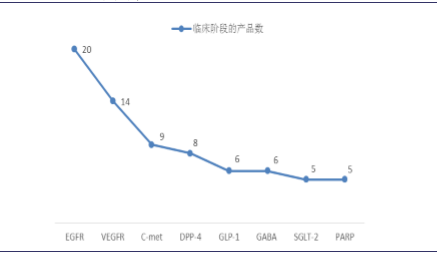
近年来,我国新药研发环境显著改善,大量海归人员不断创业,百济神州、贝达药业等企业的成功也形成了良好的示范效应;在当前国家鼓励创新、为创新药审批开辟绿色通道等政策的推动下,创新药的研发和审评周期有望进一步缩短(盐酸埃克替尼申报上市仅用时10个月),从而有效延长产品的有效生命周期;1类新药逐步纳入各地医保等也在很大程度上鼓励了新药的研发。
近年来新药研发环境显著改善
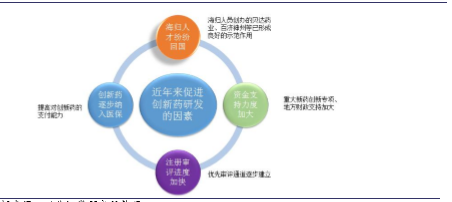
目前国内确实有一批企业在创新药方面进行了布局,如恒瑞医药、石药集团、江苏豪森、贝达药业等,国内创新药研发的热情在持续升温,取得多个里程碑式成果,多个新药也在申报中。
国内创新药研发取得多个里程碑式成果
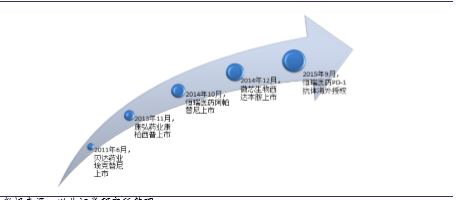
2012-2015年国内部分公司申报的1.1类新药


“十二五”以来,针对重大疾病围绕产业链部署研发链,获批24个1类新药,建成各类平台近300个,突破核心关键技术50余项,获得国家一、二等奖51项,支持产业创新孵化基地60余个,国家经费投入71.9亿,产生直接经济效益1600亿,出口产值37亿美元。生物疫苗研发水平位居世界前列,化学药物创新研究实现与国际同步,中药产业形成全球化发展趋势,促进我国医药科技由仿制向创制、医药产业由大国向强国的转变。
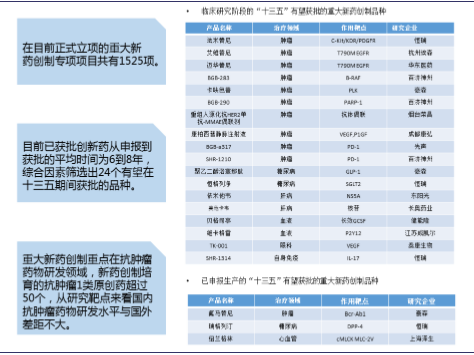
“十三五”有望获批的重大新药创制品种
本文地址:http://www.zwzyzx.com/show-262-238382-1.html
相关资讯
- 国内化学原料药及制剂行业发展挑战及不利因素(2015-06-05)
- 目前,中成药行业所处产业链条情况(2014-09-18)
- 我国医药及中药行业进入的主要壁垒(2014-06-07)
- 政府支出的持续提升及医保覆盖面的不断扩大促进药品零售发展(2015-01-18)
- 居民收入快速增长和消费升级趋势催生医疗美容需求(2016-09-09)
- 全球兽药市场保持稳定增长 达到225亿美元的市场规模(2014-07-08)
- 干细胞产业规模空间巨大(2016-11-22)
- 统治电商逻辑的“大而全”在医疗服务领域不再适用(2016-05-27)
合作媒体
最新报告
定制出版
热门报告
免责声明
中为咨询所引述的资料是用于行业市场研究以及讨论和交流,并注明出处,部分内容是由相关机构提供。若有异议请及时联系本公司,我们将立即依据相关法律对文章进行删除或作相应处理。查看详细》》



