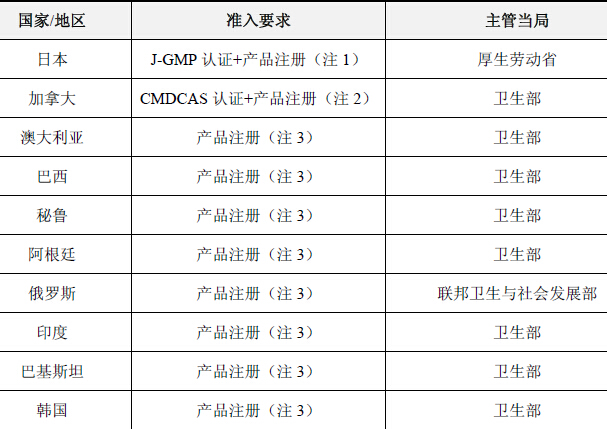
全球主要国家或地区产品准入要求总结
相关报告
- 2015-2020年中国留置导尿管行业市场深度剖析及投资前景趋势研究报告(2015-03-06)
- 2015-2020年中国血透管路行业市场深度调查研究及投资前景分析报告(2015-03-06)
- 2016-2022年中国体外循环管路区域行业市场调查研究及发展分析报告(2015-10-22)
- 2016-2022年中国医用连接管区域行业市场调查研究及发展分析报告(2015-10-22)
- 2015-2020年中国留置导尿管行业市场重点层面调查研究报告(2015-09-24)
- 中国留置导尿管行业市场深度调查研究及投资咨询报告(2018-07-19)
- 2015-2020年中国血透管路行业市场重点层面调查研究报告(2015-09-24)
- 2015-2020年中国体外循环管路行业市场发展研究及投资前景分析报告(2015-03-06)
- 中国血透管路行业市场深度调查研究及投资咨询报告(2018-07-19)
- 2016-2022年中国硅胶胃管区域行业市场调查研究及发展分析报告(2015-10-22)
主要国家或地区产品准入要求总结如下:

本文地址:http://www.zwzyzx.com/show-329-115450-1.html
上一篇:中国医疗器械注册程序情况
下一篇:国内外气管插管行业重点企业介绍
相关资讯
- 测序技术随着新的测序原理及测序仪推出迅速发展(2016-08-25)
- 国内体外诊断产品的需求量将会持续增长(2014-06-11)
- 前列地尔注射液及贝前列素钠片的市场状况(2014-08-25)
- 杜拉宝(消旋卡多曲颗粒)在消旋卡多曲颗粒剂中的市场地位(2014-07-14)
- 一次性无菌医用高分子制品原材料价格波动的影响(2014-06-21)
- 从区域分布上看,2006年至2016年全球医药市场销售情况(2014-10-20)
- 丙肝对社会危害大(2016-06-23)
- 国内分子诊断行业主管部门及监管体制(2015-08-01)
合作媒体
最新报告
定制出版
热门报告
免责声明
中为咨询所引述的资料是用于行业市场研究以及讨论和交流,并注明出处,部分内容是由相关机构提供。若有异议请及时联系本公司,我们将立即依据相关法律对文章进行删除或作相应处理。查看详细》》



