他山之石:加强监管+实质性利好,推动美国儿童药领域快速发展
相关报告
- 数据更新中...
美国作为世界儿童药品发展历史上的先锋军,在20世纪80年代之初,其市场上仅有大约20%的儿科药品进行过安全性或有效性测试,儿童用药的安全性、有效性和可及性问题也困扰着医生、患儿家长和管理当局。随后美国FDA出台一系列相应的法律和法规,一方面对儿童用药的安全性和有效性加强监管,如儿科标签法和儿科研究平等法,另一方面则在研发、专利期保护/专卖权等各个方面给予极大政策支持,成为美国儿童药领域发展的主要推动力。
美国儿童用药相关法规/政策演变过程

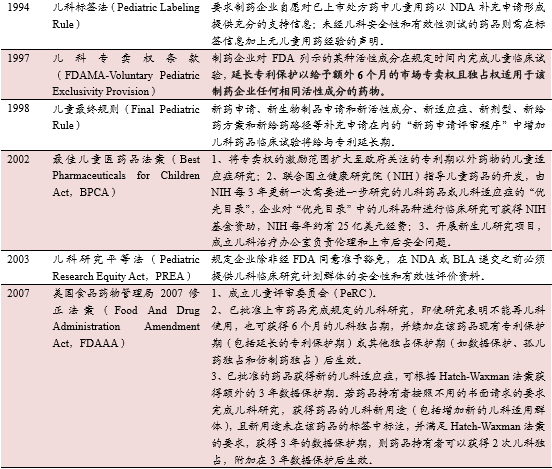
美国针对儿童药物的特殊性,在研发、注册审评审评及销售给予不同程度的政策倾斜,极大地促进儿童药物的规范化发展。根据美国FDA统计,2002-2007年间,有99项申请涉及257项儿科国际多中心临床研究,覆盖60个适应症,美国有398个临床机构参与其中178项研究,美国成为全球儿科临床研究的最大贡献者。自2007年起进行BPCA和/或PREA研究共344项,受试者合计155755例,其中按BPCA进行的研究供给130项,约占总研究项目的38%。2011年底,儿科标签信息更新的产品共有424个,386个药品进行儿科研究,72个药品表明对儿童无效,74个药品更新或强调安全性信息,33个药品给出特定的剂量调整或变更,301个产品扩大适用年龄层。2012年底,美国共有186个药物获得儿科独占权,进行BPCA和PREA而获得儿科独占权的有39个。受益于此,美国儿童药平均利润率从政策实施前的18.5%上升到35%,儿童孤儿药的利润更是高达80%以上。
本文地址:http://www.zwzyzx.com/show-329-223970-1.html
相关资讯
- 华兰生物:血制品龙头+医药工业受压下稀缺避险标的(2016-09-09)
- 全球原料药行业供求状况及变动原因(2014-08-06)
- 医药行业主要政策法规和发展规划(2014-08-07)
- 医用敷料产品进口国的市场和政策情况(2015-12-30)
- 与其他国家相比,我国医美市场渗透率仍然较低,市场空间巨大(2016-09-12)
- 2013年度福建地区医疗卫生机构门诊服务情况分析(2014-04-02)
- 国内高精度医用过滤器行业的进入壁垒(2015-01-03)
- 全球医药市场规模情况(2015-02-13)
合作媒体
最新报告
定制出版
热门报告
免责声明
中为咨询所引述的资料是用于行业市场研究以及讨论和交流,并注明出处,部分内容是由相关机构提供。若有异议请及时联系本公司,我们将立即依据相关法律对文章进行删除或作相应处理。查看详细》》



