国内与中药行业相关的法律法规和产业政策
相关报告
- 2014-2018年中国中药饮片业兼并重组及投资建议研究分析报告(2014-10-08)
- 2015-2020年中国注射用骨肽行业市场重点层面调查研究报告(2015-09-23)
- 2015-2020年中国中药饮片行业市场调查研究及投资发展分析报告(2015-05-08)
- 中国中药材行业市场深度调查研究及投资咨询报告(2018-07-17)
- 2014-2018年中国中药饮片企业拟IPO上市细分市场研究报告(2014-10-08)
- 2015-2020年中国中药制剂行业市场主要领域调查分析报告(2015-09-23)
- 2016-2022年中国中药制剂区域行业市场调查研究及发展分析报告(2015-10-21)
- 2016-2022年中国注射用血塞通行业市场深度调查研究及投资咨询报告(2015-11-19)
- 中国中药制剂行业市场深度调查研究及投资咨询报告(2018-07-17)
- 中国注射用骨肽行业市场深度调查研究及投资咨询报告(2018-07-17)
与中药行业相关的法律法规和产业政策如下:
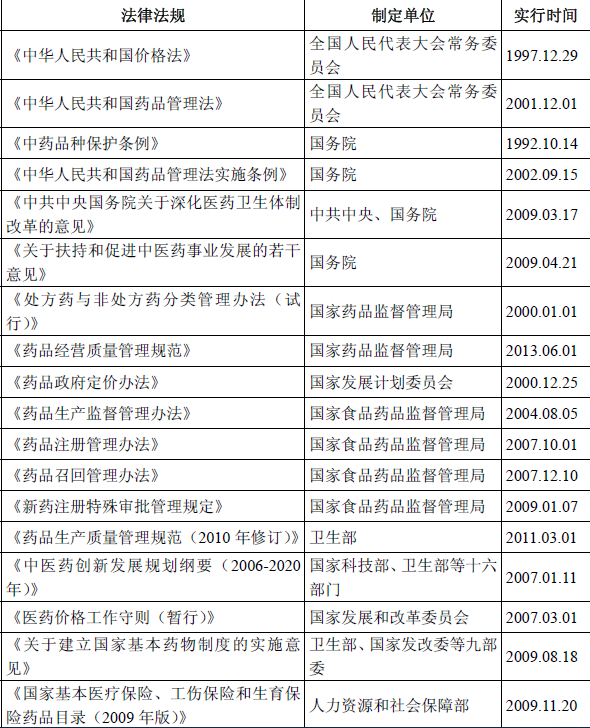
上述行业法律法规和产业政策主要规范了医药行业生产、经营等以下几个方面的管理制度:

上述行业法律法规和产业政策主要规范了医药行业生产、经营等以下几个方面的管理制度:
(1)行业准入
2001年全国人民代表大会常务委员会制定的《中华人民共和国药品管理法》对我国医药企业的行业准入进行了明确规定:
①药品生产企业准入制度
开办药品生产企业,须经企业所在地省、自治区、直辖市人民政府药品监督管理部门批准并发给《药品生产许可证》,凭《药品生产许可证》到工商行政管理部门办理登记注册。无《药品生产许可证》的,不得生产药品。
②药品经营企业准入制度
开办药品批发企业,须经企业所在地省、自治区、直辖市人民政府药品监督管理部门批准并发给《药品经营许可证》;开办药品零售企业,须经企业所在地县级以上地方药品监督管理部门批准并发给《药品经营许可证》,凭《药品经营许可证》到工商行政管理部门办理登记注册。无《药品经营许可证》的,不得经营药品。
(2)药品生产质量管理规范(GMP)和药品经营质量管理规范(GSP)
根据《中华人民共和国药品管理办法》相关规定,药品生产企业必须按照《药品生产质量管理规范》组织生产,药品监督管理部门按照规定对药品生产企业进行GMP认证,对认证合格的发给GMP证书;药品经营企业必须按照《药品经营质量管理规范》开展经营,药品监督管理部门按照规定对药品经营企业进行GSP认证,对认证合格的发给GSP证书。
(3)处方药和非处方药分类管理
根据《中华人民共和国药品管理法》的规定,我国实行处方药和非处方药分类管理制度。处方药和非处方药的分类管理是目前国际通行的药品管理模式。患者购买处方药需凭医生开具的处方,一般多为新药或临床使用复杂、监管要求较高的药品;非处方药可由患者直接在药品零售店购买,一般为治疗常见疾病且临床使用安全简单的常用药品。通过加强对处方药和非处方药的监督管理,规范药品生产、经营行为,引导公众科学合理用药,减少药物滥用和药品不良反应的发生、保护公众用药安全。
(4)药品注册管理
国家食品药品监督管理局药品注册司主管全国药品注册工作,依据国家药监局2007年公布的《药品注册管理办法》,新药研制必须按照国家药监局的规定如实报送研制方法、质量指标、药理及毒理试验结果等有关资料和样品。药品注册申请人研发新药完成临床前研究后,将相关研究资料和样品报送国家药监局,经批准获得《药物临床试验批件》,而后根据批准的临床方案分期进行临床试验,将临床试验资料及其他变更和补充资料报送国家药监局,通过审批则获得《药品注册批件》和新药证书;申请人已持有《药品生产许可证》并具备该药品相应生产条件的,进行生产前现场核查,符合要求的,可以发给药品批准文号。药品生产企业在取得药品批准文号后,方可生产该药品。
(5)药品定价
根据《中华人民共和国价格法》、《药品政府定价办法》及《医药价格工作守则》等法律、法规的规定,我国药品定价实行政府定价或政府指导价,列入国家基本医疗保险药品目录的药品以及国家基本医疗保险药品目录以外具有垄断性生产、经营的药品,实行政府定价或政府指导价;对其它药品,实行市场调节价。政府定价时,区别GMP与非GMP药品、原研制与仿制药品、新药和名优药品与普通药品定价,优质优价。根据《医疗机构药品集中招标采购试点工作若干规定》、《关于集中招标采购药品有关价格政策问题的通知》等文件规定,县级及县级以上医疗机构参照价格主管部门公布的最高零售价格和市场实际购销价格进行药品集中招标采购。
(6)中药品种保护制度
根据国务院1992年公布的《中药品种保护条例》,国家对质量稳定、疗效确切的中药品种实行保护的制度。国家药监局下属国家中药品种保护评审委员会负责对申请保护的中药品种进行评审后颁发中药保护品种证书,受保护的中药品种分为一、二级。中药一级保护品种保护期分别为三十年、二十年、十年,二级保护品种为七年;一级中药保护品种因特殊原因需要延长保护期的,由生产企业在该品种保护期满前6个月申报延长保护期申请,每次延长时间不得超过第一次批准时保护期限;中药二级保护品种在保护期满后可以延长7年,需要在保护期满前6个月申报延长保护申请。国家中药保护品种在保护期限内其他企业不得生产。
(7)行业标准
国家药品标准是指国家食品药品监督管理局颁布的《中华人民共和国药典》、药品标准、药品注册标准以及卫生部标准等,其内容包括质量指标、检验方法以及生产工艺等技术要求。药品注册标准是指国家食品药品监督管理局批准给申请人特定药品的标准,生产该药品的生产企业必须执行该注册标准,但也是属于国家药品标准范畴。我国2007年公布的《药品注册管理办法》规定药品注册标准不得低于《中国药典》的规定。
本文地址:http://www.zwzyzx.com/show-348-140756-1.html
下一篇:国内中药制剂行业进入的主要壁垒
相关资讯
- 国内汽车零部件行业主要政策法规(2015-02-03)
- 联合国贸易发展委员会对港口的分类(2014-12-29)
- 中国菜籽油市场竞争格局(2015-05-02)
- 国内临床医疗信息系统物联网技术将被广泛应用(2014-07-11)
- 我国休闲食品行业营销渠道多元化(2014-05-28)
- 国内医药行业市场供求状况及变动原因(2014-10-06)
- 国内地基与基础工程行业重点企业情况介绍(2015-04-10)
- 国内进入聚氨酯泡沫稳定剂行业的主要壁垒(2015-06-18)
合作媒体
最新报告
定制出版
热门报告
免责声明
中为咨询所引述的资料是用于行业市场研究以及讨论和交流,并注明出处,部分内容是由相关机构提供。若有异议请及时联系本公司,我们将立即依据相关法律对文章进行删除或作相应处理。查看详细》》



