临床试验资源短缺严重,期待国家开源
相关报告
- 2014-2018年中国医药行业市场发展研究及投资咨询研究报告(2014-01-04)
- 2014版全国主要地区原料药产业发展状况暨投资环境调查研究报告(2014-05-23)
- 中国特色原料药行业市场深度调查研究及投资咨询报告(2018-07-17)
- 2016-2022年中国原料药区域行业市场调查研究及发展分析报告(2015-10-21)
- 2015-2020年中国特色原料药行业运行研究及市场投资发展分析报告(2015-05-08)
- 2015-2020年中国原料药行业市场深度剖析及投资发展研究报告(2015-06-25)
- 2014-2018年中国原料药企业拟IPO上市细分市场研究报告(2013-12-10)
- 2014-2018年中国仿制药行业市场深度调查研究及投资前景分析报告(2014-05-23)
- 全国主要地区中成药制剂产业发展状况暨投资环境调查研究报告(2014-12-01)
- 2015-2020年中国中成药行业深度调研及市场投资发展研究报告(2015-06-25)
根据我们前文的测算,本次一致性评价涉及到的潜在品种数量规模巨大,如果所有品种最终都选择BE试验,受制于临床试验基地资源、受试者、样品分析和存储等因素的约束,要按时完成相关品种的评价,我们认为存在较大的压力,尤其是临床机构数量上明显不足。
药物临床试验面临四大约束
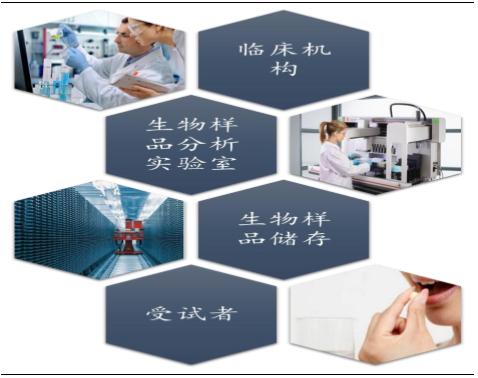
目前全国共有433家GCP证书未到期(截止2015年12月31日)的机构,而根据CDE临床试验登记平台和中国临床试验注册中心ChiCTR数据,只有122家开展过BE/I期项目,而在722临床数据自查核查风暴中有80家机构涉及。研究报告根据驭时临床试验信息截止2016年1月份对128家机构调研的信息看,只有53家机构表示可承接BE/I期项目,其中10家机构专科类机构(肿瘤类、精神类、眼科),从临床机构资源看,目前面临较大的压力。
BE临床试验机构承接情况

监管层或将适度放开GCP资格,市场分析根据我们从产业链和业内人士了解,监管部门有可能会对药物临床试验机构资格认定有条件的放开,我们认为开放和推进国内BE基地认证、再认证将使得目前国内BE基地资源相对短缺的现状得到改善。但从风险控制角度看,我们预计大面积放开的可能性不大,预计将会设定相应的硬性指标,如医院级别、相关专业能力等。目前已有山东省提出“积极争取国家相关部委支持,在山东省布局增设I期临床试验室。协调相关部门,调动医疗机构、临床医师开展临床试验的积极性,满足一致性评价工作需要。”(鲁食药监药注„2016‟59号)
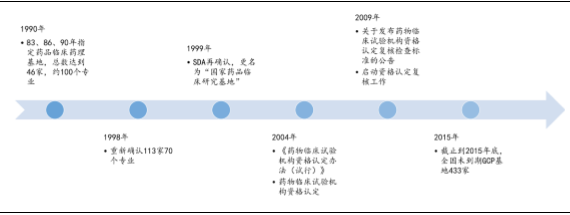
药物临床试验机构状况:目前约430家GCP基地
本文地址:http://www.zwzyzx.com/show-262-243362-1.html
上一篇:药学研究或成企业主要障碍
相关资讯
- 国内医药行业与上下游行业之间的关联性及影响(2015-01-25)
- 小儿止咳中成药市场发展情况(2015-07-23)
- 国内医药行业的管制特征(2015-04-08)
- 国内妇科用药市场情况(2014-09-18)
- 国内注射用还原型谷胱甘肽钠市场竞争状况(2014-11-23)
- 全球皮肤病用药市场的容量在各类药物市场中排名第九(2014-10-20)
- 医疗:体制改革,提高医疗服务价格(2016-04-22)
- 人体微量元素检测市场竞争格局和发展趋势(2015-08-25)
合作媒体
最新报告
定制出版
热门报告
免责声明
中为咨询所引述的资料是用于行业市场研究以及讨论和交流,并注明出处,部分内容是由相关机构提供。若有异议请及时联系本公司,我们将立即依据相关法律对文章进行删除或作相应处理。查看详细》》



