国内医药行业主要法律法规汇总
相关报告
- 2015-2020年中国中成药制剂行业深度调研及市场投资发展研究报告(2015-06-26)
- 2014-2018年抗感染药项目商业计划书(2014-10-09)
- 2015-2020年中国中成药行业运行研究及市场投资发展分析报告(2015-05-08)
- 2014-2018年中国中成药行业市场全面深度调查研究及投资研究报告(2013-12-29)
- 2014-2018年中国中成药制剂业兼并重组及投资建议研究分析报告(2014-10-09)
- 2014-2018年中国抗感染药行业市场深度调查研究及投资前景分析报告(2014-09-12)
- 2014-2018年中国中成药业兼并重组及投资建议研究分析报告(2014-10-08)
- 2015-2020年中国中成药制剂行业运行研究及市场投资发展分析报告(2015-05-12)
- 2015-2020年中国抗感染药行业市场深度剖析及投资发展研究报告(2015-06-26)
- 2014-2018年中成药项目商业计划书(2014-10-09)
国家制定了严格的法律法规来规范医药行业,主要有:
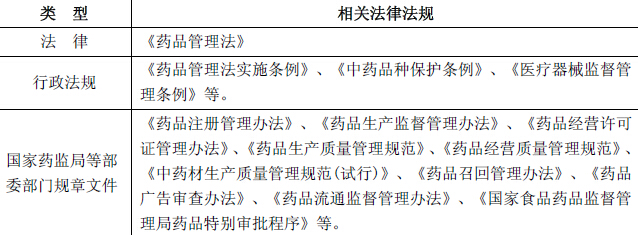
其中:《药品管理法》(2001 年2 月28 日修改)规定了药品的研制、生产、经营、使用和监督管理必须遵守相关规定,目的在于加强药品监督管理,保证药品质量,保障用药安全,维护人民群众身体健康和用药的合法权益。

《药品管理法实施条例》(2002 年8 月4 日公布)规定了对药品生产企业管理、药品经营企业管理、医疗机构的药剂管理、药品管理、药品包装的管理、药品价格和广告的管理、药品监督等进行了详细规定。
《药品生产监督管理办法》(2004 年8 月5 日公布)的立法目的在于加强药品生产的监督管理,依法对药品生产条件和生产过程进行审查、许可进行监督检查。
《药品注册管理办法》(2007 年6 月18 日发布)对药物临床试验、药品生产或者进口、药品注册检验以及监督管理进行了具体规定,目的在于保证药品的安全、有效和质量可控,规范药品注册行为。
《药品生产质量管理规范(2010 年修订)》(卫生部令第79 号)即新版GMP自2011 年3 月1 日起施行,对药品生产质量管理、机构和人员、厂房与设施、设备、物料与产品、确认与验证、文件管理、生产管理、质量控制与质量保证、委托生产与委托检验、产品发运与召回、自检等生产相关方面作了系统规定,新版GMP 的标准达到了世界卫生组织药品GMP 的要求。新版GMP 施行后,新建药品生产企业、药品生产企业新建(改、扩建)车间应符合新版GMP 的要求;现有药品生产企业将给予不超过5 年的过渡期,并依据产品风险程度,按类别分阶段达到新版GMP 的要求。
《药品经营质量管理规范》(卫生部令第90 号)即新版GSP 自2013 年6 月1 日起施行,该规范是对我国医药流通政策的一次较大调整,新版GSP 的修订借鉴和吸收了WHO、欧盟GDP 的管理理念和方法,如供应链理念、企业信息化管理、物流技术与应用、质量风险管理、冷链管理及验证、体系内审等,将我国药品经营质量管理与国际药品流通质量管理的通行做法逐步接轨。随着新版GSP的出台,市场准入门槛得到提高,有望抑制企业低水平重复现象,以促进行业结构调整,提高市场集中度,促进药品流通领域的规范和健康。
本文地址:http://www.zwzyzx.com/show-329-94038-1.html
上一篇:国内医药行业监管体制
下一篇:近期国内医药行业主要相关产业政策
相关资讯
- 国家政策的支持医用敷料的发展(2015-12-29)
- 中国医疗IT行业发展情况(2016-03-21)
- 药品销售渠道变革:网售处方药破冰利好商业企业(2016-07-15)
- 三甲医院虚假宣传遭起底(2016-11-04)
- 中国成为全球医疗器械制造中心之一(2016-04-29)
- 新博柴黄(柴黄颗粒)技术水平及特点(2014-07-14)
- 医药行业“品牌移植”的得与失(2016-05-11)
- 医药行业的周期性、区域性或季节性特征(2015-01-25)
合作媒体
最新报告
定制出版
热门报告
免责声明
中为咨询所引述的资料是用于行业市场研究以及讨论和交流,并注明出处,部分内容是由相关机构提供。若有异议请及时联系本公司,我们将立即依据相关法律对文章进行删除或作相应处理。查看详细》》



